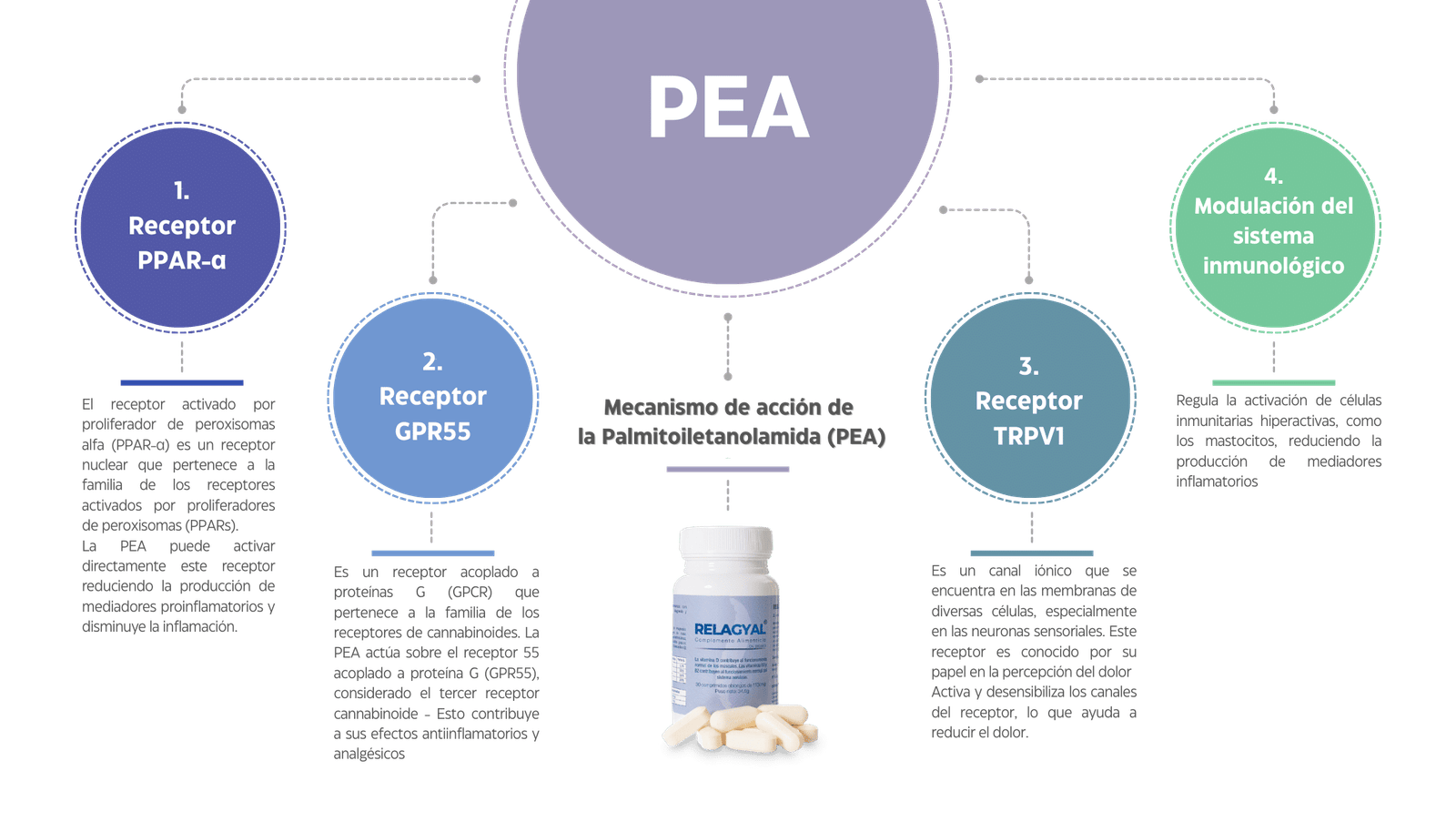
El mecanismo de acción de la PEA (palmitoiletanolamida) ha sido un tema muy estudiado desde su descubrimiento en el año 1957 por el científico italiano Angelo Raffaele Mezzanzanica.
La PEA es un compuesto natural que se encuentra en varios alimentos y también es producida por el cuerpo humano, es una amida de ácido graso con propiedades antiinflamatorias, analgésicas y neuroprotectoras. Su mecanismo de acción es complejo y multifacético, involucrando varias vías celulares.
Se ha demostrado que la regulación de las células no neuronales y, por lo tanto, el control de la neuroinflamación depende de la síntesis local «bajo demanda» de la amida lipídica endógena palmitoiletanolamida y los endocannabinoides relacionados. Cuando el equilibrio entre la síntesis y la degradación de este mediador lipídico bioactivo se interrumpe en favor de una síntesis reducida y/o una mayor degradación, el comportamiento de las células no neuronales puede no estar adecuadamente regulado y la neuroinflamación excede los límites fisiológicos. En estas condiciones el aumento de la palmitoiletanolamida endógena, ya sea disminuyendo su degradación o administrándola de forma exógena, es capaz de mantener la neuroinflamación dentro de sus límites fisiológicos.
Mecanismo de Acción de la PEA
-
Modulación del sistema endocannabinoide
- No se une directamente a los receptores cannabinoides CB1 y CB2, pero potencia los efectos de la anandamida (AEA) al inhibir su degradación por la enzima FAAH (fatty acid amide hydrolase).
- Esto prolonga la actividad de la AEA, que activa los receptores CB1 y CB2, produciendo efectos analgésicos y antiinflamatorios.
-
Activación del receptor nuclear PPAR-α (Peroxisome Proliferator-Activated Receptor Alpha)
- La PEA actúa como agonista de PPAR-α, un receptor clave en la regulación de la inflamación y el dolor.
- Su activación reduce la liberación de mediadores inflamatorios como la interleucina-1β (IL-1β), TNF-α y la COX-2.
- También disminuye la activación de mastocitos y microglía, células clave en el dolor neuropático.
-
Efecto en canales iónicos y neurotransmisores
- Inhibe la sobreexcitación neuronal al modular canales de sodio y calcio, reduciendo la liberación de glutamato (neurotransmisor excitatorio).
- Puede interactuar con receptores TRPV1 (receptor de potencial transitorio vanilloide 1), involucrados en la transmisión del dolor.
-
Neuroprotección y modulación de la glía
- Reduce la activación de la microglía y los astrocitos, que desempeñan un papel en la inflamación del sistema nervioso central.
- Disminuye el daño oxidativo y el estrés celular en neuronas y tejidos inflamados.
Conclusiones
El mecanismo de acción de la PEA se basa en su efecto a través de múltiples vías, principalmente mediante la activación de PPAR-α, la modulación del sistema endocannabinoide, la inhibición de la activación de mastocitos y microglía, y la regulación de la excitabilidad neuronal. Esto la hace útil en el tratamiento del dolor crónico, neuropático e inflamatorio.
Referencias bibliográficas que respaldan la información sobre el mecanismo de acción de la PEA o palmitoiletanolamida:
- Petrosino, S., & Di Marzo, V. (2017). «The pharmacology of palmitoylethanolamide and first data on the therapeutic efficacy of some of its new formulations.» British Journal of Pharmacology, 174(11), 1349-1365. citeturn0search5
- Clayton, P., et al. (2021). «Palmitoylethanolamide: a natural compound for health management.» International Journal of Molecular Sciences, 22(9), 5272. citeturn0search5
- Gabrielsson, L., Mattsson, S., & Fowler, C. J. (2016). «Palmitoylethanolamide for the treatment of pain: pharmacokinetics, safety and efficacy.» British Journal of Clinical Pharmacology, 82(4), 932-942. citeturn0search5
- Keppel Hesselink, J. M., & Hekker, T. A. (2012). «Therapeutic use of the endogenous fatty acid amide palmitoylethanolamide (PEA) in depression: a translational study.» Lipids in Health and Disease, 11, 1-7. citeturn0search5
- Impellizzeri, D., et al. (2014). «Palmitoylethanolamide reduces inflammation and pain in a mouse model of spinal cord injury.» Journal of Neuroinflammation, 11, 122. citeturn0search5